全球CAR-T療法第一梯隊(duì) 10款體內(nèi)研發(fā)管線盤點(diǎn)與生物技術(shù)開發(fā)趨勢
嵌合抗原受體T細(xì)胞(CAR-T)療法在血液腫瘤治療中已取得革命性成功,但傳統(tǒng)的體外制備流程復(fù)雜、成本高昂、生產(chǎn)周期長。為突破這些瓶頸,全球生物技術(shù)公司正競相開發(fā)“體內(nèi)”(in vivo)CAR-T療法,即通過直接將基因遞送載體注射到患者體內(nèi),在體內(nèi)對T細(xì)胞進(jìn)行原位工程化改造。這有望將CAR-T療法轉(zhuǎn)化為一種更便捷、可及性更高的“現(xiàn)成”治療模式。以下盤點(diǎn)了目前處于全球研發(fā)第一梯隊(duì)的10款體內(nèi)CAR-T臨床在研管線,并探討其背后的技術(shù)路徑與開發(fā)生態(tài)。
第一梯隊(duì)體內(nèi)CAR-T臨床在研管線盤點(diǎn)
- CAP-001(Capstan Therapeutics)
- 技術(shù)平臺:基于脂質(zhì)納米顆粒(LNP)遞送mRNA,靶向CD19。其核心是將編碼CAR的mRNA和靶向T細(xì)胞的配體共同封裝于LNP中,LNP在體內(nèi)將mRNA選擇性遞送至T細(xì)胞,實(shí)現(xiàn)瞬時(shí)CAR表達(dá)。
- 開發(fā)階段:臨床前/早期臨床階段,專注于自身免疫性疾病(如系統(tǒng)性紅斑狼瘡)的探索。
- CB-010(Caribou Biosciences)
- 技術(shù)平臺:利用CRISPR-chRDNA基因編輯技術(shù)和腺相關(guān)病毒(AAV)載體遞送。旨在通過一次治療,在體內(nèi)同時(shí)敲除T細(xì)胞的PD-1基因并插入靶向CD19的CAR序列,以增強(qiáng)抗腫瘤活性。
- 開發(fā)階段:已進(jìn)入針對B細(xì)胞非霍奇金淋巴瘤的I期臨床試驗(yàn)(ANTLER研究)。
- 體內(nèi)CAR-T項(xiàng)目(Ensoma)
- 技術(shù)平臺:基于工程化腺病毒(Engenious? AAV)載體,能夠高效感染造血干細(xì)胞和祖細(xì)胞(HSPCs)及T細(xì)胞,實(shí)現(xiàn)長期、穩(wěn)定的基因修飾。目標(biāo)是實(shí)現(xiàn)“一次治療,終身受益”。
- 開發(fā)階段:臨床前開發(fā)中,與武田(Takeda)合作推進(jìn)。
- VOR33(Vor Biopharma)
- 技術(shù)平臺:雖然嚴(yán)格意義上不是典型的體內(nèi)CAR-T,但其思路具有啟發(fā)性。通過體外編輯造血干細(xì)胞(敲除CD33),回輸后產(chǎn)生對CD33靶向療法(如抗體藥物偶聯(lián)物)“免疫”的血液系統(tǒng),從而在治療AML時(shí)保護(hù)健康細(xì)胞。其體內(nèi)策略正在探索中。
- 開發(fā)階段:相關(guān)技術(shù)處于臨床開發(fā)階段。
- 體內(nèi)CAR-T項(xiàng)目(Intellia Therapeutics)
- 技術(shù)平臺:憑借其在體內(nèi)CRISPR基因編輯領(lǐng)域的領(lǐng)先地位,Intellia正探索將LNP遞送的CRISPR系統(tǒng)與CAR基因模板結(jié)合,在體內(nèi)對T細(xì)胞基因組進(jìn)行精準(zhǔn)整合。
- 開發(fā)階段:臨床前研究階段。
- IMC-001(Immatics與Bristol Myers Squibb合作)
- 技術(shù)平臺:基于T細(xì)胞受體(TCR)的體內(nèi)療法,使用病毒載體將腫瘤特異性TCR基因遞送至患者T細(xì)胞。雖然非CAR結(jié)構(gòu),但代表了體內(nèi)工程化T細(xì)胞療法的另一重要分支。
- 開發(fā)階段:早期臨床開發(fā)中。
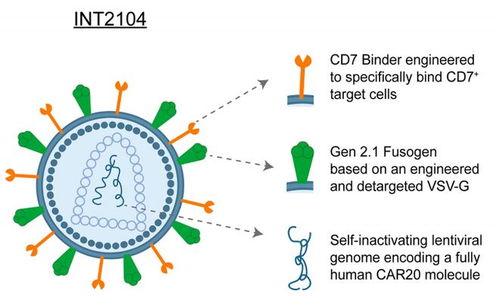
- 體內(nèi)CAR-T項(xiàng)目(Sana Biotechnology)
- 技術(shù)平臺:開發(fā)低免疫原性的病毒載體(如Fusogenix載體),旨在逃避宿主免疫系統(tǒng)的中和,實(shí)現(xiàn)重復(fù)給藥和高效體內(nèi)基因遞送至T細(xì)胞。
- 開發(fā)階段:臨床前開發(fā)階段。
- ARTEMIS?平臺衍生項(xiàng)目(Adicet Bio與馴鹿生物合作)
- 技術(shù)平臺:雖然主力是通用型(異體)CAR-T,但其平臺技術(shù)(如特定的CAR結(jié)構(gòu))和基因工程能力為未來開發(fā)體內(nèi)遞送策略奠定了基礎(chǔ)。
- 開發(fā)階段:同種異體現(xiàn)有管線已進(jìn)入臨床,體內(nèi)方向在研。
- 體內(nèi)CAR-T項(xiàng)目(Beam Therapeutics)
- 技術(shù)平臺:利用其堿基編輯(Base Editing)技術(shù),無需切斷DNA雙鏈即可實(shí)現(xiàn)精確的單堿基修改。正探索通過LNP將堿基編輯器和CAR模板遞送入體內(nèi),對T細(xì)胞進(jìn)行多重編輯,以創(chuàng)建更安全、高效的體內(nèi)CAR-T。
- 開發(fā)階段:臨床前研究階段。
- ACD項(xiàng)目(Allogene Therapeutics)
- 技術(shù)平臺:作為通用型CAR-T的領(lǐng)導(dǎo)者,Allogene已布局“現(xiàn)成”體內(nèi)CAR-T(稱為ACD)。其思路可能是利用其先進(jìn)的異體細(xì)胞平臺技術(shù)與體內(nèi)基因遞送相結(jié)合,實(shí)現(xiàn)終極的“現(xiàn)成藥”模式。
- 開發(fā)階段:早期研發(fā)階段。
核心技術(shù)路徑與生物技術(shù)開發(fā)挑戰(zhàn)
當(dāng)前體內(nèi)CAR-T的開發(fā)主要圍繞三大核心技術(shù)展開競爭:
- 病毒載體(特別是AAV):優(yōu)勢是轉(zhuǎn)導(dǎo)效率高,可實(shí)現(xiàn)長期表達(dá);挑戰(zhàn)是免疫原性、載體容量限制和潛在的基因組整合風(fēng)險(xiǎn)。
- 非病毒載體(主要是LNP-mRNA):優(yōu)勢是安全性高(瞬時(shí)表達(dá))、可重復(fù)給藥、生產(chǎn)工藝相對簡單;挑戰(zhàn)是靶向特異性、體內(nèi)遞送效率和對T細(xì)胞的持久性改造能力。
- 基因編輯工具(CRISPR、堿基編輯等)整合:旨在實(shí)現(xiàn)CAR基因的定點(diǎn)、穩(wěn)定整合,同時(shí)可敲除免疫抑制基因(如PD-1),但技術(shù)復(fù)雜,脫靶效應(yīng)和安全性是關(guān)注重點(diǎn)。
開發(fā)生態(tài)與未來趨勢:
跨界融合:該領(lǐng)域呈現(xiàn)出mRNA技術(shù)、基因編輯、載體工程與免疫學(xué)深度交叉融合的特點(diǎn)。新興生物技術(shù)公司(如Capstan, Caribou)與大型藥企(如BMS, 武田)通過合作加速推進(jìn)。
適應(yīng)癥拓展:早期探索已從血液腫瘤延伸至自身免疫性疾病、纖維化疾病等,潛力巨大。
* 核心挑戰(zhàn):精準(zhǔn)的體內(nèi)T細(xì)胞靶向、可控的CAR表達(dá)時(shí)長與水平、避免對非靶細(xì)胞的編輯、以及最終的成本與可及性,仍是研發(fā)需要攻克的堡壘。
###
體內(nèi)CAR-T療法代表了細(xì)胞治療范式的下一次重大演進(jìn)。盡管目前多數(shù)管線尚處于早期階段,臨床轉(zhuǎn)化的道路上面臨諸多科學(xué)和工藝挑戰(zhàn),但其一旦成功,將徹底改變細(xì)胞治療的格局,使其真正成為一種可規(guī)模化、可負(fù)擔(dān)的常規(guī)治療選擇。第一梯隊(duì)的競爭已經(jīng)展開,未來幾年關(guān)鍵的臨床概念驗(yàn)證數(shù)據(jù)將成為行業(yè)發(fā)展的風(fēng)向標(biāo)。
如若轉(zhuǎn)載,請注明出處:http://m.udca.cn/product/62.html
更新時(shí)間:2026-03-13 08:04:25